赛默飞战略合作伙伴 诺禾致源多基因检测试剂盒获批成功
发布时间:2018-08-19作者:赛默飞世尔科技(中国)有限公司
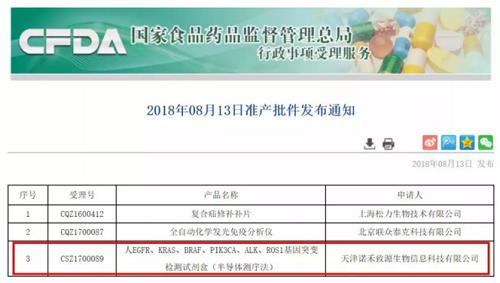
近日,国家药品监督管理局通过创新医疗器械特别审批通道,批准天津诺禾致源生物信息科技有限公司“人EGFR、KRAS、BRAF、PIK3CA、ALK、ROS1基因突变检测试剂盒(半导体测序法)”的三类医疗器械产品上市。
用于检测非小细胞肺癌(NSCLC)患者肿瘤组织中与靶向治疗密切相关的六个基因的突变状态,筛选适合接受靶向药物治疗的患者。据悉,该试剂盒基于DA8600二代测序平台,是目前国内唯一仪器和试剂均获批的NGS肿瘤检测系统。也是目前已获批产品中基因数目最多、位点最多、报告周期最短的试剂盒。
中国临床肿瘤学会《原发性肺癌诊疗指南》指出:
“ KRAS、PIK3CA突变与EGFR-TKI耐药有关,可通过NGS技术进行检测。诺禾致源的多基因检测试剂盒覆盖与NSCLC靶向治疗用药相关的六个基因,是目前CNDA批准的最多基因的肿瘤分子检测试剂盒,全面提示患者治疗相关的敏感、潜在耐药及基因共突变信息,能够准确提示基因丰度。”
与传统基因检测手段相比,基于NGS技术的多基因检测试剂盒,只需一份组织样本、一次检测即可覆盖多个肿瘤治疗相关基因,实现点突变、插入缺失、重排(融合)等多种变异形式的检测,为医生和患者提供更全面的靶向治疗的解决方案。
该多基因检测试剂盒经过北京肿瘤医院、北京胸科医院、华西医院、中国人民解放军总医院和河南省肿瘤医院共5个中心2789例样本的临床试验验证。该检测试剂盒与传统金标准检测方法的比较研究结果显示,总符合率均在99%以上。
与吉非替尼、奥西替尼、克唑替尼伴随诊断试剂的比较研究结果显示,该多基因检测试剂盒与原有伴随诊断试剂具有良好的检测一致性。与吉非替尼、奥西替尼、克唑替尼药物疗效相关的回顾性临床研究结果显示,根据该试剂盒检测结果用药的NSCLC患者,客观缓解率(ORR)与既往药物临床试验ORR相符。通过以上临床性能的全面研究,充分证明了该多基因检测试剂盒在NSCLC患者靶向治疗用药指导中的重要价值。
本次获批上市的多基因检测试剂盒基于扩增子建库与半导体测序的技术体系开发,该技术体系已获得国际认可。
基于该技术的仪器也就是DA8600高通量基因测序仪是由达安基因股份有限公司引进赛默飞的技术,在国内研发、生产、面向临床应用的新一代高通量测序仪,已于2017年1月获得国家食品药品监督管理总局的注册批准(国械注准20143401961),可以用于肿瘤和遗传疾病等人体基因位点的检测。
这是目前中国首台由CFDA批准的可用于肿瘤和遗传疾病临床检测的高通量测序仪,可广泛应用于各医疗机构临床检测中心。
该仪器可实现从样本提取到上机测序在一天内完成;
配合DA Chef系统,可实现全自动化模板制备和芯片上样工作流程。
该仪器对环境要求相对较低、通量适中、检测周期较短的优势,特别适合在医院内开展肿瘤检测。2017年6月,基于该技术体系的OncomineDx Target Text试剂盒获FDA批准上市,全球最大规模的临床试验NCI-MATCH也采用了该技术体系。

DA8600高通量基因测序仪
此次基于DA8600开发的多基因检测试剂盒的获批,是诺禾致源布局肿瘤NGS分子诊断领域的重要起点。此前,诺禾致源围绕该检测试剂盒进行了一系列的DNA提取备案,“癌症基因数据处理软件”III类医疗器械的申报等,结合此次多基因检测试剂盒的获批,力图为医院提供一站式肿瘤NGS分子病理诊断整体解决方案。
赛默飞作为诺禾致源的重要战略合作伙伴,受邀出席了其上市发布会,祝贺诺禾致源实现此历史性突破,未来赛默飞亦将全方位继续支持诺禾致源在该领域的发展,持续提供稳定可靠的产品和服务,与诺禾致源一起致力于服务中国肿瘤患者人群,进而助力改善人类生活。
Copyright © 2015 ilinki.net Inc. All rights reserved. 智汇工业版权所有
电话:010-62314658 邮箱:service@ilinki.net
 主办单位:智汇万联(北京)信息技术有限公司
主办单位:智汇万联(北京)信息技术有限公司

